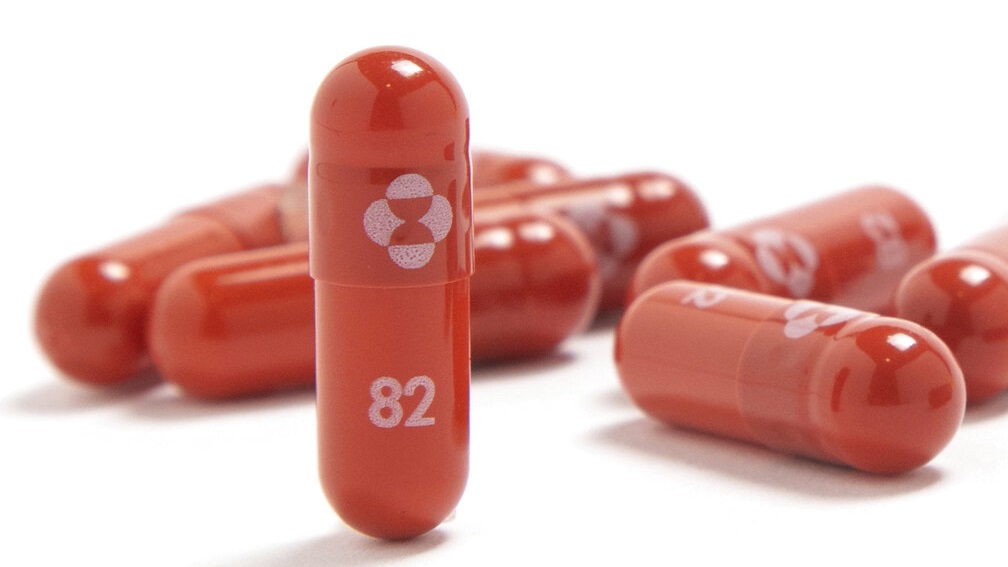
美國食品藥物管理局(FDA)周四核准默沙東藥廠開發的新冠口服藥Molnupiravir,這是繼核准輝瑞口服藥Paxlovid之後,又一獲放行的新冠肺炎口服藥。FDA批准Molnupiravir口服藥可用來治療有嚴重疾病風險的成人之輕症至中度新冠肺炎症狀。
FDA在官網提到,「Molnupiravir 只能以處方樂物方式向病人開出;病人應在確診後、出現病狀的5日內展開療程。」FDA又提到,18歲以下者不可以接受Molnupiravir療程,因為Molnupiravir骨骼及軟骨的生長。此外,FDA也指出,由於在動物測試中顯示,Molnupiravir會對胚胎造成傷害,所以不建議孕婦服用。
然而,由於Molnupiravir試驗數據並不符合預期,法國衞生部長韋朗(Olivier Veran)周一宣布取消訂單,成為全球首個放棄採用Molnupiravir的國家。法國先前向默沙東訂了夠5萬份療程用的Molnupiravir。韋朗稱,政府會付退訂的賠償費,他又指,政府採購了輝瑞研發的Paxlovid,但沒有透露數量,「法國已在排隊購買,明年1月底前到貨。」

法國衞生部長韋朗周一宣布取消Molnupiravir訂單。路透社資料圖片